千葉大学大学院薬学研究院薬効薬理学准教授
藤野 裕道
はじめに

人類が薬の人工合成に初めて成功したのは19世紀の終わりでした。その薬の名前はアセチルサリチル酸、現在でも世界中で使われているアスピリンです。21世紀に入ってアスピリンの服用が、大腸癌の予防や予後改善に効果があるのではないか、との報告が見られるようになりました。
アスピリンは、シクロオキシゲナーゼ(COX)を阻害しプロスタグランジンの産生を抑制します。プロスタグランジンは炎症反応などの引き金となる生理活性物質です。このプロスタグランジンの産生亢進が、大腸癌患者で報告されています。このことからアスピリンの効果は、プロスタグランジンの産生を抑制し、その癌細胞への作用を阻害するためだと考えられています。
プロスタグランジンは、それ自体で作用することは極めて少なく、「受容体」
を介して生体反応を引き起こします。われわれはプロスタグランジン受容体の細胞内情報伝達系を研究することで癌メカニズムの解明を目指しています。
EP4受容体とEP2受容体‐2つは似て非なる受容体?
EP受容体は、主要なプロスタグランジンであるプロスタグランジンE2(PGE2)の受容体であり、大きく分類して4つのサブタイプが存在します。われわれは、その中のEP4およびEP2受容体に注目しました。
それぞれの遺伝子がクローニングされて以来、これら2つの受容体サブタイプは、同じリガンドやGαsタンパク質を共有しているため、薬理学的には同等に扱われていました。われわれは、これら2つの受容体サブタイプの役割分担の違いを解明するため、それぞれの受容体を発現させたモデル細胞を用いて解析を進めました。
その結果、EP4およびEP2受容体は、大腸癌への関与が知られているβカテニン情報伝達系を、それぞれ異なる経路を介して活性化することを明らかとしました。特にEP4受容体はPI3キナーゼを主に介してβカテニン系を活性化しますが、その系によりPGE2合成酵素発現も誘導する可能性を示しました。
さらにこの系は、百日咳毒素感受性であることからGαi型蛋白質も、Gαs型蛋白質のほかにEP4受容体と共役していることを見出しました。すなわちEP4受容体は、EP2受容体では活性化されない付加的な情報伝達系を介して癌化に関与している可能性が示されました。
大腸癌とEP4受容体、そしてEP3受容体‐癌悪性化の鍵となる受容体?
EP4受容体と癌との関係をさらに明らかにするため、ヒト結腸癌細胞株HCA-7細胞を用いて、内在的なEP4受容体系の詳細を解析しています。
現在までに、EP4受容体はGαi型蛋白質/PI3キナーゼ系の活性化を介して、プロスタグランジン合成の要となるCOX-2発現を癌細胞において誘導することや、そのメカニズムなどを明らかとしました。
つまりEP4受容体を活性化させると、COX-2が発現し、それにより新たなPGE2の産生が亢進します。そのPGE2により、再びEP4受容体が活性化されるポジティブ・フィードバック機構が形成され、癌の悪性化が亢進する可能性が考えられます。
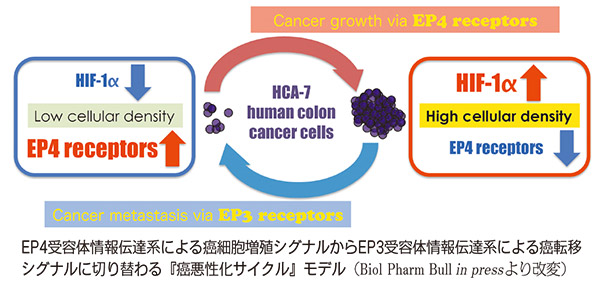
ところが癌細胞密度が高くなるにつれて、低酸素状態に応答して機能する低酸素誘導因子1α(HIF-1α)が増加し、EP4受容体発現とCOX-2発現が減少することも見出しました。一方で、高細胞密度条件下で培養したHCA-7細胞において、EP3受容体サブタイプの活性化により細胞の移動能が亢進すること、すなわちEP3受容体は、転移を制御している可能性も見出しました。
癌悪性化サイクル‐癌のネガティヴ・スパイラル・メカニズム?
ここで、一つの疑問が生じます。HCA-7細胞の増殖に伴うEP4受容体の減少とCOX-2発現の低下、そしてEP3受容体による細胞移動の亢進など、一見脈絡のない結果は何を意味しているのでしょうか。
一つの解釈として、「癌細胞増殖シグナルが、癌転移シグナルに切り替わるメカニズム」ではないかと、われわれは考えています。つまり高密度になるまで増殖した癌細胞は、EP4受容体による細胞増殖を停止し、EP3受容体による転移を誘発します。
転移先での癌細胞は、細胞密度が低下するため移動をやめ、再びEP4受容体数を増加させ細胞増殖を促進する『癌悪性化サイクル』を形成する可能性が示唆されます。
EP2受容体とDP受容体‐EP2受容体は代替不可?
さてEP4受容体と癌との関係性は、ある程度明らかとなりましたが、EP2受容体はどうなのでしょうか。実はプロスタノイド受容体の系統樹では、EP2受容体は同じリガンドを共有するEP4受容体よりも、進化的にはプロスタグランジンD2(PGD2)受容体であるDP受容体に近いことが示されています。
この2つの受容体遺伝子は、ヒトでは同じ14番染色体上に並んでおり、遺伝子重複によって生じたと考えられています。これら受容体のアミノ酸変異について、ヒトゲノム・データベースを使用し比較解析したところ、EP2受容体にはDP受容体と比べて、変異しているアミノ酸が非常に少ないことが解りました。
つまり、EP2受容体は変異に対して何らかの制約を受けていることが考えられます。すなわちEP2受容体は生体維持に関して代用が利かない役割を担っていることが考えられます。
おわりに
癌を含めた様々な病態へのプロスタグランジン受容体情報伝達系の詳細な解析により、治療につながるターゲットの絞り込みに関して、大きな貢献ができることが考えられます。
そして将来的に、予防へと結びつく有益な情報を提供できる可能性を期待して、われわれは現在も鋭意に研究を進めています。